Exame cada vez mais presente nos tratamentos de reprodução assistida, a análise genética do embrião na FIV pode trazer informações valiosas para aumentar as chances de sucesso de gravidez por transferência embrionária e reduzir riscos de anomalias.
Com os avanços da medicina reprodutiva, entender quando e porque utilizar a estratégia de análise genética é possível e possibilita a transferência da FIV para a gestação mais segura, melhorando a experiência do casal e o potencial de concepção.
Neste conteúdo, produzido pela Dra. Taiane Andrade (CRM 52 103847-8 RJ | RQE 31779 | RQE 58467), ginecologista especializada em reprodução assistida pela FEBRASGO e AMB, você vai descobrir em quais situações a análise genética embrionária é recomendada, quais são seus principais benefícios e como ela pode contribuir para o planejamento reprodutivo.
O que é a análise genética do embrião na FIV?
Também conhecida como teste genético pré-implantacional (PGT) , a análise genética do embrião na fertilização in vitro (FIV) consiste em um exame realizado antes da transferência do embrião para o útero. O objetivo da FIV com análise genética dos embriões é avaliar se há alterações cromossômicas ou genéticas.
No exame, a partir de uma amostra de células, é possível identificar embriões euploides, que são aqueles que têm os cromossomos normais. Esses embriões podem ter maior chance de implantação e desenvolvimento saudável, reduzindo o risco de falhas de implantação, abortos ou doenças genéticas hereditárias.
Importante dizer que os termos anteriores “diagnóstico genético pré-implantacional (PGD)” e “rastreio genético pré-implantacional (PGS)” foram substituídos pelo termo “teste genético pré-implantacional (PGT)”, após uma revisão da terminologia utilizada no tratamento da infertilidade.¹
O que é analisado no teste genético pré-implantacional?
Na biópsia em embriões, que é o procedimento mais usado no Brasil quando falamos de PGT, são analisadas anormalidades genéticas. Isso inclui PGT para aneuploidia (PGT-A), PGT para doenças monogênicas/de gene único (PGT-M) e PGT para rearranjos cromossômicos estruturais (PGT-SR).1
O PGT é um teste realizado para analisar o DNA de oócitos (corpúsculos polares) ou de embriões (estágio de clivagem ou blastocisto). Pode ser usado para tipagem HLA (Antígeno Leucocitário Humano – que identifica proteínas na superfície das células para avaliar compatibilidade) ou para determinar anormalidades genéticas.
Como é feita a biópsia embrionária?
O procedimento de biópsia pré-implantacional de embriões consiste em duas etapas principais:
- criar uma abertura na zona pelúcida (ZP), que é a “casquinha do embrião”;
- e aspirar algumas células da camada externa do blastocisto, chamada trofectoderma (TE).
O laser é, atualmente, o método mais usado para a abertura da ZP para biópsias de estágio de clivagem e blastocisto.
Para biópsia de blastocisto, a aspiração dentro da micropipeta de biópsia e excisão com laser podem ser usadas. Durante o procedimento, as células são coletadas em pequenos tubos (do inglês, “tubing”) para os testes com amplificação de genoma completo (WGA) como primeiro passo. Outra forma de extrair as células da biópsia é a aspiração em pequenos tubos em combinação com o desprendimento mecânico das células do trofectoderma (chamado de “flicking”).1
A análise embrionária é segura?
Sim, é segura. A biópsia embrionária é um procedimento realizado em laboratório, nos embriões no estágio de blastocisto (cerca de 5 a 7 dias após a fecundação), em geral.
Nessa fase, o embrião já possui centenas de células, e o embriologista retira algumas delas da parte externa (que dará origem à placenta), sem comprometer a estrutura que formará o bebê.
Após a coleta, o embrião é preservado enquanto o material é enviado para a análise genética de embriões, permitindo a avaliação antes da transferência para o útero da mãe que gerará o bebê.
Em que momento do processo ocorre ?
A biópsia pode ser realizada pela remoção de um ou dois blastômeros no estágio de clivagem ou pela remoção de algumas (5 a 10) células do trofectoderma no estágio de blastocisto.
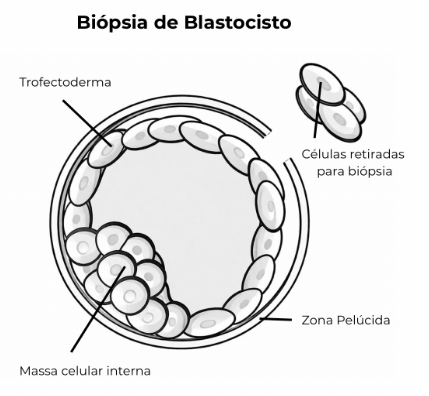
Imagem autoral com ajuda de AI em referência a fonte do artigo 1
Embora a biópsia em estágio de clivagem tenha sido a forma mais praticada de biópsia para análise embrionária por mais de uma década, seu uso clínico foi reduzido. Atualmente, a biópsia de blastocisto ou biópsia de trofectoderma (TE) é a técnica mais utilizada. Ela fornece mais células e está em um estágio embrionário mais adequado para análise genética e menos sensível a possíveis danos. Após a biópsia do TE, a criopreservação do embrião é geralmente obrigatória, devido ao tempo necessário para o resultado.1
Para que (e quem) a análise genética do embrião é indicada?
A idade materna avançada é uma das principais indicações. Além dela, as seguintes indicações para o uso da análise genética foram relatadas:
- idade materna avançada;
- falha de implantação recorrente;
- fator masculino grave;
- perda gestacional recorrente.
Importante explicar neste ponto que o fator masculino grave é uma combinação de oligospermia (baixa concentração de espermatozoides), astenozoospermia (baixa motilidade espermática) e/ou teratozoospermia (morfologia espermática anormal) ou azoospermia.
Já a perda gestacional recorrente foi recentemente desconsiderada como indicação, a não ser que haja uma anomalia conhecida no cariótipo parental. Deve-se notar que casais com esse histórico têm uma alta chance de conceber naturalmente com sucesso. Assim, o PGT-A para perda gestacional sem causa genética não é recomendado em diretriz recente baseada em evidências (The ESHRE Guideline Group on RPL et al., Updated 2023).
Desse modo, o acompanhamento com especialista em fertilidade no Rio de Janeiro, ou em sua região, é essencial para identificar em quais casos o exame de rastreio genético é indicado e como podem ajudar na futura gestação.
Para que serve a análise genética embrionária?
O PGT-A tem sido realizado em pacientes de fertilização in vitro (FIV) com o objetivo de aumentar as taxas de gravidez por transferência de embrião e diminuir as taxas de aborto espontâneo. Outras medidas de resultado, como o aumento da transferência eletiva de embrião único e a redução do tempo para a gravidez, foram adicionadas mais recentemente.1
O percentual de diagnósticos incorretos é muito baixo, em torno de 1% a 3%, sendo um procedimento bastante confiável.2
Além disso, pode ser aplicado em situações como as descritas abaixo:
Detectar alterações cromossômicas (aneuploidias)
O teste genético é um método válido para detectar alterações cromossômicas em meiose e mitose.
A meiose é o processo de divisão celular que originam os gametas. Os erros neste processo, principalmente na formação dos óvulos, são avaliados de forma confiável a partir da biópsia do TE. Defeitos na meiose resultam em aneuploidia, ou seja, células com número anômalo de cromossomos.
Já a mitose é a divisão celular que ocorre nas células do corpo, e não nas reprodutivas. Os erros neste processo levam ao mosaicismo cromossômico (presença tanto de células com número normal quanto de células com número anômalo de cromossomos no mesmo embrião).
Erros na mitose podem ser detectados dentro de determinadas limitações técnicas, metodológicas e biológicas. A taxa estimada de diagnósticos inconclusivos deve ser inferior a 5%.
Apesar de apresentarem taxas de implantação baixas, embriões mosaicos podem dar origem tanto a bebês normais quanto a bebês sindrômicos, dependendo do grau de mosaicismo e do cromossomo afetado. Portanto, muitas vezes, este diagnóstico pode gerar dúvidas em relação à viabilidade do embrião.De forma geral, a biópsia de blastocisto permite realizar múltiplas análises para diferentes indicações, a partir da mesma amostra após a WGA (por exemplo, anormalidades cromossômicas e variantes patogênicas) de maneira eficiente.1
Identificar doenças genéticas específicas
Algumas doenças genéticas são determinadas por uma alteração do DNA chamada variante patogênica, apresentando um único gene anômalo. Por isso, são chamadas de doenças monogênicas.
PGT-M é o teste para variantes patogênicas de DNA que causam doenças monogênicas, ligadas ao cromossomo X, autossômicas dominantes ou recessivas, para as quais os loci causadores da doença (nucleares ou mitocondriais) foram inequivocamente identificados.
Assim, o teste de PGT-M detecta variantes patogênicas que apresentam alta probabilidade de causar doenças com graves efeitos na saúde que podem manifestar-se no nascimento, na infância ou na idade adulta.2
Alguns exemplos clássicos dessas condições, em que pode ser útil a aplicação do PGT-M, são fibrose cística, anemia falciforme, doença de Huntington, hemofilia e distrofia muscular de Duchenne.
Reduzir falhas de implantação
Falhas na implantação podem resultar em perda gestacional. E a aneuploidia embrionária representa a principal causa de perda gestacional precoce, pois os blastocistos aneuploides apresentam uma capacidade de desenvolvimento reduzida e um potencial de implantação muito baixo.
Estudos de caso-controle demonstraram que anomalias do cariótipo são mais frequentes em pacientes com falha de implantação recorrente, mesmo que a prevalência absoluta (2,1%) seja baixa.
Os valores estão dentro da faixa de prevalência de anormalidades cromossômicas descritas em casais inférteis submetidos a técnicas de reprodução assistida, variando de 2,8% a 12% em homens e de 3,0% a 15% em mulheres. Com relação ao tipo de anormalidades do cariótipo em casais com falha de implantação recorrente estão:
- anormalidades autossômicas;
- aberrações dos cromossomos sexuais;
- mosaicismo cromossômico.
Portanto, a contribuição do cariótipo parental anormal na predisposição a erros cromossômicos nos embriões é plausível, apesar da maioria das aneuploidias cromossômicas embrionárias ter origem durante a formação do óvulos (meiose).
Dessa forma, caso uma anormalidade cromossômica seja detectada no casal, recomenda-se aconselhamento genético e, quando relevante, teste genético pré-implantacional (PGT) para reduzir esses riscos.3
Perda gestacional recorrente ou abortamento de repetição
A aneuploidia é uma causa reconhecida de perda gestacional e perda precoce com riscos aumentados conforme a idade da mulher. As aneuploidias ocorrem com frequências comparáveis tanto em mulheres com perda gestacional esporádica quanto recorrente.
A perda gestacional subsequente dependerá da natureza da anomalia presente no cariótipo parental, com mais perdas gestacionais em portadoras de translocações recíprocas e inversões em comparação com translocações robertsonianas ou outros tipos de anomalias.
Importante dizer que, mesmo que uma anomalia no cariótipo parental seja encontrada, as taxas cumulativas de nascidos vivos são boas, assim como as chances de um filho saudável, apesar de um risco maior de perda gestacional.
A discussão com base no histórico de alterações genéticas na família ajudará na tomada de decisões sobre continuar tentando engravidar, parar de tentar ou optar por testes invasivos, como o diagnóstico pré-natal ou o teste genético pré-implantacional (PGT) (por exemplo, PGT-SR em caso de translocação balanceada).
Vale dizer que o PGT-SR pode reduzir a taxa de aborto espontâneo, mas não melhorará a taxa de nascidos vivos ou o tempo necessário para engravidar.
Contudo, estudos sobre a aplicação do teste genético para aneuploidia (PGT-A) nos casos de perda gestacional recorrente e sua real influência no sucesso gestacional e taxas de nascidos vivos não demonstram um benefício claro.
Assim, são necessárias mais informações precisas sobre as vantagens e desvantagens do PGT-A no abortamento de repetição, considerando erros de diagnóstico e a falta de evidências de que ele melhore a taxa de nascidos vivos, pois a qualidade geral das evidências ainda é muito baixa. 4
Casais que têm um filho que necessita de transplante
Em caso de análise de compatibilidade para transplantes, o diagnóstico genético com PGT também é uma estratégia válida para avaliar a compatibilidade de um embrião com o irmão.
Assim, quando todas as outras opções clínicas se esgotarem, a seleção de embriões com compatibilidade HLA (Human Leukocyte Antigen), via PGT, é aceitável.
Essa estratégia pode ser indicada para casais que já têm um filho afetado por uma doença maligna adquirida ou uma doença genética, em que a criança afetada provavelmente será curada ou a expectativa de vida será prolongada pelo transplante com células-tronco de um irmão HLA compatível.
O teste pode ser realizado apenas para tipagem HLA se o risco de recorrência da doença for baixo, ou em combinação com doenças autossômicas dominantes/recessivas ou ligadas ao cromossomo X.
Deve-se atentar para o tempo necessário para a preparação do PGT, aplicação do(s) ciclo(s) de FIV e para o nascimento de um irmão HLA compatível. Portanto, os casos em que a criança afetada apresenta uma condição médica aguda que impossibilite o transplante seguro de células-tronco ou uma expectativa de vida extremamente baixa devem ser cuidadosamente considerados para o PGT.
Qualquer solicitação de tipagem HLA para criar um futuro doador para um irmão na ausência de uma doença específica deve ser recusada.2
Afinal, quando fazer análise genética do embrião na FIV?
As indicações para o PGT incluem idade materna avançada, falha de implantação recorrente e fator masculino grave. 1 Já para o abortamento recorrente, a recente diretriz européia sobre o assunto mostra que a indicação da análise genética é discutível.4
A análise genética aumenta as chances de gravidez?
A análise genética do embrião na FIV pode, sim, aumentar a chance de gravidez por transferência de embrião. Isso porque o teste genético permite identificar quais embriões têm maior probabilidade de implantação. Ao selecionar embriões sem alterações cromossômicas, o processo se torna mais assertivo, reduzindo tentativas com embriões que dificilmente evoluiriam.
Por outro lado, é importante entender que a análise genética não aumenta a taxa de gestação cumulativa do casal, isto é, não aumenta a probabilidade total de engravidar após múltiplos ciclos de tratamento de reprodução assistida.
Além disso, esse exame não melhora a qualidade do embrião. Isso quer dizer que ele não “corrige” alterações e nem torna um embrião que já apresenta anomalias em um embrião viável para a transferência, ou seja, apenas avalia quais já apresentam os cromossomos normais ou anormais.
Além disso, a análise genética não garante a gravidez. Mesmo com a escolha de um embrião euploide (cromossomicamente normal), outros fatores, como idade, estilo de vida e fatores de infertilidade do casal também influenciam no sucesso do tratamento.
Na prática, o principal benefício é permitir uma seleção mais precisa, aumentando as chances de sucesso por transferência de embrião na FIV e contribuindo para o planejamento reprodutivo.
Existem riscos na análise genética do embrião?
A análise genética do embrião é segura e amplamente utilizada na fertilização in vitro, mas, como qualquer etapa do tratamento, não é isenta de riscos.
O principal aspecto é que o exame pode apresentar resultados inconclusivos ou situações como o mosaicismo (quando um mesmo embrião apresenta células normais e células alteradas), o que pode dificultar a tomada de decisão. Isso porque embriões mosaico podem resultar tanto em bebês normais, como em bebês sindrômicos, dependendo do grau de mosaicismo, e do cromossomo afetado.
Dessa forma, é uma situação muito delicada que exige assinatura de termo de consentimento, aconselhamento por geneticista e a realização de um pré-natal mais atento.
Outra situação que pode ocorrer, especialmente na idade materna avançada, é de não haver embrião euploide disponível para transferência, mesmo após inúmeros ciclos de FIV. Isso pode ser bastante frustrante, quando todos os embriões obtidos são aneuploides.
Além disso, a análise genética não elimina outros riscos gestacionais, já que fatores como condições uterinas e aspectos clínicos da paciente também influenciam no sucesso da gravidez e nascimento de um bebê vivo e saudável.
Por isso, a indicação deve sempre ser individualizada, com orientação médica especializada, após discutir riscos e benefícios.
Como é feita a decisão sobre fazer ou não o PGT?
A decisão deve ser considerada após discussão e avaliação em conjunto com o especialista em reprodução assistida, para identificar a prática mais indicada e os possíveis resultados.
De acordo com a Dra. Taiane Andrade (CRM 52 103847-8 RJ | RQE 31779 | RQE 58467), especialista em reprodução assistida pela FEBRASGO e AMB e Membro da Sociedade Brasileira de Reprodução Assistida (SBRA), o aconselhamento deve ser amplo, por exemplo:
“Os custos e os prazos também devem ser discutidos para que os pacientes estejam informados sobre todos os aspectos da FIV com PGT antes de iniciar o tratamento. O impacto social e psicológico também precisa ser considerado, especialmente em casais já responsáveis pelos cuidados de filhos afetados.”
Aconselhamento sobre o tratamento de FIV
Segundo a Dra Taiane Andrade (CRM 52 103847-8 RJ | RQE 31779 | RQE 58467), em relação ao tratamento de FIV, o aconselhamento deve incluir discussão sobre:
- número de óvulos coletados e a necessidade de maximizar esse número, ou seja, acumular óvulos para a FIV com PGT-A (dentro dos limites seguros);
- número de embriões viáveis esperados para biópsia e a porcentagem esperada de “sobrevivência” embrionária;
- possibilidade de algum embrião apresentar diagnóstico inconclusivo. Em casos específicos, uma nova biópsia é aceitável para obter um diagnóstico;
- possibilidade de não haver embriões para transferência se todos os embriões forem geneticamente anômalos;
- probabilidade de gravidez/nascimento de um bebê vivo por ciclo iniciado e por transferência de embrião, levando em consideração a idade materna e a indicação;
- risco de aborto espontâneo e a importância da reanálise do tecido placentário ou fetal para avaliar taxas de falso negativo e tratamentos adicionais;
- opções para embriões não transferidos ou congelados para uso futuro, incluindo doação para pesquisa, de acordo com as regulamentações locais.
Em todo caso, se nenhum diagnóstico for obtido, a seleção dos embriões para transferência não é aceitável. Uma exceção pode ser feita para o PGT-A, mas requer o consentimento da paciente.2
Aconselhamento sobre a análise genética
Relacionado à análise genética, o aconselhamento deve incluir discussão sobre:
- revisão atualizada do risco genético e confirmação molecular ou citogenética do diagnóstico, quando apropriado, a gravidade e a variabilidade da condição e a presença ou ausência de correlação genótipo/fenótipo;
- princípio do teste, no qual deve ser explicado que, dependendo da indicação, amostras biológicas e relatórios genéticos do casal e de familiares relevantes podem ser necessários para a análise laboratorial;
- condição(ões) testada(s), o método de teste e as limitações do teste;
- prazo previsto para a análise laboratorial e o tratamento;
- comunicação dos resultados e a política do centro sobre achados incidentais;
- tomada de decisão sobre quais embriões são aceitáveis para transferência/vitrificação (antes do início de um ciclo de tratamento e pode precisar ser revisto);
- destino de embriões não diagnosticados e embriões não transferíveis;
- mosaicismo cromossômico como um fenômeno biológico inerente em embriões humanos e, quando apropriado, como isso pode afetar o diagnóstico e a política de transferência de embriões do centro;
- possibilidade de um diagnóstico incorreto.
Quanto ao último tópico, taxas de erro expressas como resultados falso-negativos ou falso-positivos devem ser baseadas em análises internas e de acompanhamento para testes ou estratégias diagnósticas específicas.2
Palavra da especialista
“A análise genética do embrião é uma ferramenta importante na fertilização in vitro, mas deve ser indicada com critério e de forma individualizada. Ela ajuda a tomar decisões mais assertivas ao identificar quais embriões têm maior potencial de implantação, contribuindo para o sucesso da FIV.
Contudo, essa não é uma garantia de gravidez, mas uma estratégia que pode aumentar a taxa de sucesso por transferência de embrião. Por isso, a avaliação médica é essencial para entender quando esse recurso faz sentido no planejamento reprodutivo e para oferecer apoio em toda a jornada da fertilidade junto à paciente.
Por isso, devemos considerar riscos, idade e chance de sucesso, reduzindo a necessidade de exames desnecessários.”
— Dra. Taiane Andrade (CRM 52 103847-8 RJ | RQE 31779 | RQE 58467), ginecologista especialista em reprodução assistida
Jornada mais tranquila: importância do acompanhamento especializado na FIV
Ao longo do tratamento de fertilização in vitro, cada decisão faz diferença e entender quando a análise genética do embrião é realmente indicada pode tornar essa jornada mais tranquila. Como vimos, esse recurso não é necessário em todos os casos, mas pode ser um grande aliado ao ajudar na escolha do embrião com maior potencial de implantação.
Se você está considerando iniciar um tratamento ou quer entender qual é o melhor caminho para o seu caso, contar com uma avaliação personalizada pode ser o primeiro passo para uma jornada mais tranquila e consciente.
Agende sua consulta com a Dra. Taiane Andrade para um acompanhamento humanizado e entenda as possibilidades para a sua jornada da fertilidade.
Perguntas Frequentes (FAQ – análise genética do embrião)
Referências
1 ESHRE PGT Consortium and SIG Embryology good practice recommendations for polar body and embryo biopsy for PGT†; ESHRE PGT Consortium and SIG-Embryology Biopsy Working Group, Georgia Kokkali 1,*,‡, Giovanni Coticchio 2,*,‡; Fernando Bronet 3, Catherine Celebi 4, Danilo Cimadomo 5, Veerle Goossens 6, Joanna Liss 7, 8, Sofia Nunes 9, Ioannis Sfontouris 10, 11 Nathalie Vermeulen 6, Elena Zakharova 12, and Martine De Rycke 13, 14. Human Reproduction Open, pp. 1–12, 2020. http://doi:10.1093/hropen/hoaa020. Disponível em https://pubmed.ncbi.nlm.nih.gov/32500104/
2 ESHRE PGT Consortium good practice recommendations for the organisation of PGT†
ESHRE PGT Consortium Steering Committee, Filipa Carvalho 1 , Edith Coonen 2, 3, Veerle Goossens 4, Georgia Kokkali 5, Carmen Rubio 6, Madelon Meijer-Hoogeveen 7, Céline Moutou 8,Nathalie Vermeulen 4, and Martine De Rycke 9, 10. Human Reproduction Open, pp. 1–12, 2020. http://doi:10.1093/hropen/hoaa021. Disponível em: https://pubmed.ncbi.nlm.nih.gov/32524036/
3 ESHRE good practice recommendations on recurrent implantation failure†; ESHRE Working Group on Recurrent Implantation Failure, D. Cimadomo 1, M.J. de los Santos 2, G. Griesinger 3, 4, G. Lainas 5, N. Le Clef 6, D.J. McLernon 7, D. Montjean 8, B. Toth9, N. Vermeulen 6, and N. Macklon 10. Human Reproduction Open, 2023, 2023(3), hoad023. https://doi.org/10.1093/hropen/hoad023.
4 Recurrent Pregnancy Loss Guideline of European Society of Human Reproduction and Embryology Update 2022. ESHRE Recurrent Pregnancy Loss Guideline Development Group. Ruth Bender Atik, Ole Bjarne Christiansen, Janine Elson, Astrid Marie Kolte, Sheena Lewis, Saskia Middeldorp, Saria Mcheik, Braulio Peramo, Siobhan Quenby, Henriette Svarre Nielsen, Marie-Louise van der Hoorn, Nathalie Vermeulen, Mariëtte Goddijn. Human Reproduction Open, Volume 2023, Issue 1, 2023. https://doi.org/10.1093/hropen/hoad002



